欢迎您访问爱非克(深圳)生物科技有限公司
关键词:AKK菌、AKK菌格林汁
代谢功能障碍相关的脂肪肝(MAFLD)是一种以大量脂质蓄积为特征的代谢综合征,包括单纯性脂肪变性(NAFL)、非酒精性脂肪性肝炎(NASH)、纤维化和肝硬化,甚至肝细胞癌(HCC)。MAFLD已成为一种主要的肝脏疾病,在全球成年人中的患病率为22-29%,其中超过75%的人超重和肥胖。然而,迄今为止,还没有获批的药物可用于MAFLD治疗。
肠道细菌AKK菌因其在治疗代谢紊乱方面的潜力而得到越来越多的认可,研究表明,通过直接用AKK菌治疗或通过饮食或药物干预增加其在肠道中的丰度,可有效治疗MAFLD。
该研究通过使用高脂肪和高胆固醇(HFC)饮食诱导的肥胖小鼠为模型,评估了AKK菌的治疗特性,同时运用代谢组学分析鉴定与MAFLD治疗相关的重要代谢物来研究AKK菌的分子作用模式。
研究内容
将7-8周龄的C57BL/6小鼠(18-20 g)饲养在无特定病原体的环境中,并按照标准化方法在22 ± 1 ℃下以12小时光/暗循环饲养,可自由获取食物和水。
在适应环境1周后,小鼠随意饲喂60%高脂肪和1.2%胆固醇(HFC)饮食17周,HFC喂养的小鼠在第11周被随机分成两亚组:接受磷酸盐缓冲液(PBS,对照组)或A. muciniphila治疗(处理组),分别处理6周。A. muciniphila溶解在无氧的PBS后最终浓度为1×108 CFU/ml,每隔一天给予小鼠悬浮液200 μL。对照组小鼠给药相同体积的PBS。
另外,对于无菌小鼠模型,在第11周前1周,HFC小鼠口服抗生素混合物Abx(含有氨苄青霉素 0.2 g/L、万古霉素 0.2 g/L、硫酸新霉素0.2 g/L和甲硝唑0.2 g/L),然后再接受单独的Abx或A. muciniphila治疗6周。Abx溶解在饮用水中。每天监测小鼠体重。
研究结束后,小鼠禁食8小时并通过i.p.注射80 mg/kg氯胺酮和10 mg/kg甲苯噻嗪进行麻醉。当小鼠完全麻醉后,取出眼球收集血液样本用于测量肝脏相关酶,收集肝脏组织测定甘油三酯(TG)和二酰基甘油(DAG),并且进行组织学检查和免疫组织化学评估以及免疫印迹分析,从粪便样本中提取细菌DNA进行16S rRNA测序,收集肝脏中的代谢物进行代谢组学分析,通过L-天冬氨酸ELISA试剂盒测量肝脏、粪便和血浆中的L-天冬氨酸水平。
研究结果
灌胃A. muciniphila减轻肥胖小鼠的MAFLD
检查HFC小鼠粪便中肠道微生物群的组成发现,HFC小鼠和A. muciniphila处理的HFC小鼠的两个不同集群显示两组之间微生物群落结构存在显著差异。α-多样性分析显示A. muciniphila灌胃增加了小鼠体内肠道菌群的丰富度和多样性,并改善微生物群落结构。值得注意的是,通过LEfSe分析,A. muciniphila被鉴定为杰出的微生物群成分之一。
接下来评估A. muciniphila在HFC饮食喂养诱导的肥胖小鼠模型中治疗MAFLD的效果,定量聚合酶链反应(qPCR)结果显示,与HFC组小鼠相比,A. muciniphila处理有效地使肠道中A. muciniphila的丰度增加了20倍,这种活动导致小鼠体重下降,A. muciniphila治疗6周后HFC小鼠体重下降约20.8%。有趣的是,A. muciniphila治疗通过降低肝TG有效减轻HFC小鼠的肝脂肪变性,在肥胖小鼠中用A. muciniphila治疗显著降低肝脏中DAG的水平。测定血浆中肝脏特异性酶的水平显示,A. muciniphila显著改善HFC小鼠的肝损伤,天冬氨酸转氨酶(AST)、丙氨酸转氨酶(ALT)和碱性磷酸酶(ALP)水平都降低。此外,病理检查进一步证实A. muciniphila在改善小鼠MAFLD的所有表型方面的治疗作用。
为了探索A. muciniphila的这些抗MAFLD作用是否依赖于药物治疗,HFC小鼠用A. muciniphila口服治疗6周后再停用A. muciniphila 4周。有趣的是,A. muciniphila戒断导致其抗MAFLD活性的有效持久性,戒断后小鼠体重、肝脏TG水平以及血浆AST、ALT和ALP水平显著降低。病理检查进一步证实A. muciniphila戒断导致小鼠持续抗MAFLD活性。A. muciniphila处理的HFC小鼠中的这些保持治疗效果与A. muciniphila丰度更高相关。
为进一步确定A. muciniphila在抗生素(Abx)处理的HFC小鼠中的抗MAFLD特性,在小鼠中用Abx处理降低A. muciniphila的丰度及其在肠道中增殖,这导致小鼠肝损伤和MAFLD表现加重,如Abx处理的HFC小鼠肝脏重量增加、肝脏TG大量积累和肝损伤。此外,与HFC小鼠或Abx处理的HFC小鼠相比,Abx+A. muciniphila共同处理组仍有显著的MAFLD衰减作用。基因表达分析进一步证实A. muciniphila下调FAS、ACC、TNF-ɑ、IL-6和MCP1基因的表达水平。综上所述,用A. muciniphila治疗可有效减轻小鼠的MAFLD。

图1 A. muciniphila减轻由HFC饮食喂养诱导的肥胖MAFLD
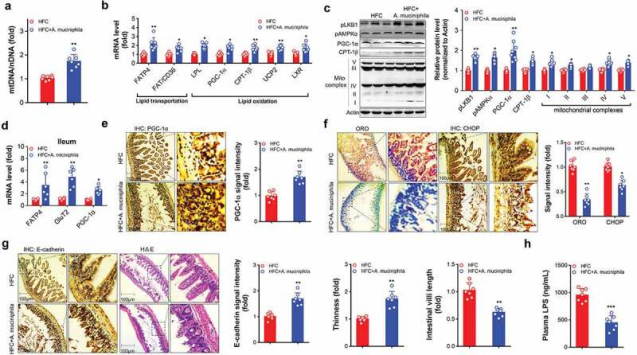
图2 A. muciniphila增加与HFC小鼠肝脏和肠道脂质代谢相关的标志物
A. muciniphila激活肠-肝轴中的脂质氧化并维持肠道屏障完整性
用A. muciniphila处理的小鼠表现出线粒体拷贝数增加,并且激活参与肝脏脂质转运[脂肪酸转运蛋白4(FATP4),脂肪酸转位酶/分化簇36(FAT/CD36)]和氧化[脂蛋白脂肪酶(LPL),过氧化物酶体增殖物激活受体γ 辅激活因子1ɑ(PGC-1ɑ)、解偶联蛋白2(UCP2)、肉碱棕榈酰转移酶1β(CPT-1β)和肝X受体(LXR)]的基因网络。免疫印迹分析显示,在小鼠中用A. muciniphila治疗激活肝激酶B1(LKB1)-AMPK轴,并增加肝脏中能量代谢调节因子(PGC-1ɑ和CPT-1β)和线粒体复合物(I、II、IV和V)的表达。
A. muciniphila减轻肥胖小鼠肠肝轴胆汁酸代谢功能障碍
探索A. muciniphila对肠-肝轴胆汁酸代谢的调节作用发现,A. muciniphila治疗导致肝脏中与胆固醇转运相关基因的表达水平增加,如低密度脂蛋白受体(LDLR),这表明A. muciniphila治疗能促进小鼠肝脏中胆固醇的转运,同时还激活一个参与胆汁酸合成和运输的基因。另外,灌胃A. muciniphila后HFC小鼠回肠和肝脏中胆汁酸调节基因的表达水平增加,如ASBT、IBABP、OSTβ、NTCP和OATP。此外,A. muciniphila治疗增强胆固醇转运[Niemann-Pick型C1样细胞内胆固醇转运蛋白1(NPC1L1)的水平增加]并降低回肠中胆汁酸合成相关基因的表达水平。与胆固醇转运调节因子(LDLR)表达水平的改变一致,A. muciniphila处理降低HFC小鼠血浆和肝脏中胆固醇的水平,表明A. muciniphila有利于肠-肝轴的胆汁酸代谢。此外,用A. muciniphila治疗的小鼠结肠中编码粘蛋白的基因mucin 2、mucin 4、mucin 5ac、mucin 5b和mucin 20的表达水平增加,粘蛋白是A. muciniphila在肠道中生长和增殖的关键底物,这一结果与之前的报道一致。
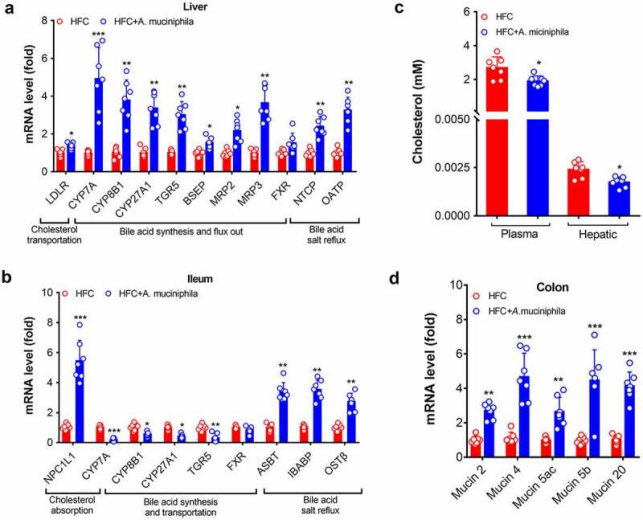
图3 A. muciniphila促进HFC小鼠肝脏和肠道中胆汁酸的代谢
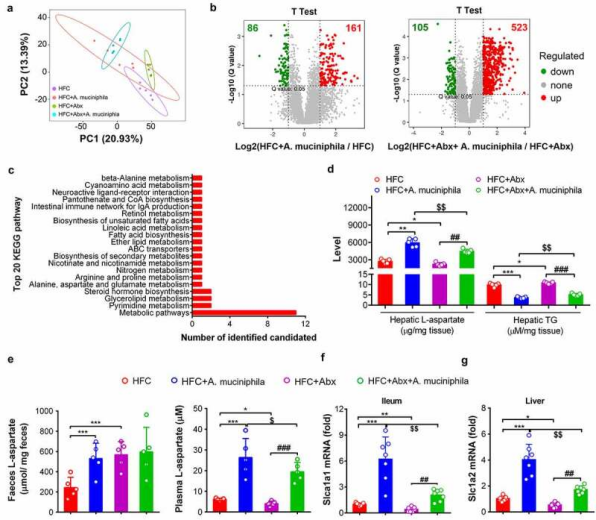
图4 A. muciniphila增加HFC小鼠肝脏中的 L-天冬氨酸水平
A. muciniphila通过促进L-天冬氨酸从肠道转运来增加肝脏L-天冬氨酸水平
代谢组学分析肝脏中的代谢特征发现,主坐标分析(PCA)显示HFC+A. muciniphila(与HFC组相比)、HFC+Abx(与HFC组相比)和HFC+Abx+A. muciniphila(与HFC+Abx组相比)的化学成分存在显著差异。与HFC小鼠相比,用A. muciniphila处理的小鼠表现出不同的代谢特征,检测到247种具有显著差异的代谢物(86种下调和161种上调),根据KEGG数据库对鉴定的代谢物进行分类,总共有98种代谢物被归入前20个KEGG二级通路;此外,与单独用Abx治疗的HFC小鼠相比,在A. muciniphila+Abx组的肝脏中检测到更显著不同的代谢物,总共检测到628种显着不同的代谢物(105种下调,523种上调),这些改变的代谢物被注释为与肝脏代谢相关,如脂肪分解、脂肪消化和吸收、胰岛素抵抗和胆汁酸生物合成。
进一步测定血浆和粪便中L-天冬氨酸的水平发现,A. muciniphila治疗有效地增加了血浆和粪便中的L-天冬氨酸水平,而Abx处理也增加粪便中的L-天冬氨酸水平,但降低血浆和肝脏中的L-天冬氨酸水平。L-天冬氨酸转运蛋白(Slc1a1或Slc1a2)在回肠或肝脏中的基因表达表明,用A. muciniphila治疗的小鼠Slc1a1 或 Slc1a2的表达水平增加,而Abx处理后L-天冬氨酸转运蛋白的表达水平降低,并部分地消除A. muciniphila对增加L-天冬氨酸转运蛋白基因表达的刺激作用。
L-天冬氨酸直接激活脂质氧化和LKB1-AMPK轴
通过在体外模拟肝脂肪变性的细胞模型,在油酸(OA)诱导的情况下将L-天冬氨酸暴露于肝细胞(L-02细胞),TG测定和尼罗红染色发现添加L-天冬氨酸有效降低了细胞脂质水平,这种减少发生在代谢能量调节因子(PGC-1α)和线粒体复合物的表达水平增加以及LKB1-AMPK轴的激活,导致氧化应激的抑制,活性氧(ROS)水平降低。这种有益的代谢作用也在OA诱导的肠细胞中出现。这些新发现与L-天冬氨酸在激活HCT-116细胞中LKB1-AMPK 轴中的代谢作用非常吻合。
为了进一步阐明L-天冬氨酸在体内的直接代谢作用,小鼠口服L-天冬氨酸24小时,结果表明L-天冬氨酸转运蛋白基因的表达在转录水平被有效激活,导致肝脏中L-天冬氨酸水平的增加。此外,L-天冬氨酸治疗激活与肝脏能量氧化相关的基因网络,如PGC-1α、UCP2和CPT-1β。PGC-1α和UCP2的免疫组织化学分析进一步证实L-天冬氨酸在肝脏中的直接代谢有益作用,这些代谢改善导致内源性肝TG水平略有降低,而没有肝损伤。
然后探讨了L-天冬氨酸在MAFLD中的治疗效果,正如预期的那样,在HFC小鼠中灌胃L-天冬氨酸(200 mg/kg)有效地防止肝脏重量增加并改善肝损伤和肝脂肪变性。HFC小鼠肝脏TG水平的定量和血浆肝脏特异性酶水平(AST、ALT、ALP)的测定进一步证实L-天冬氨酸在体内的抗MAFLD活性,表明L-天冬氨酸是治疗MAFLD的有效药物。
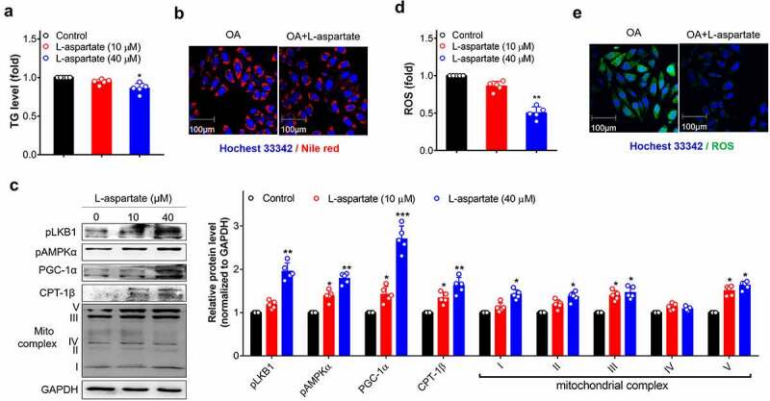 图 L-天冬氨酸可降低肝细胞中的脂质和ROS,同时增加LKB1-AMPK活性和线粒体氧化能力
图 L-天冬氨酸可降低肝细胞中的脂质和ROS,同时增加LKB1-AMPK活性和线粒体氧化能力
结论
用A. muciniphila治疗的小鼠有效逆转了肥胖小鼠肝脏中的MAFLD,如肝脂肪变性、炎症和肝损伤。这些治疗效果在长期停药后仍然存在,并且在抗生素处理的肥胖小鼠中略有减弱。A. muciniphila治疗有效地增加了肠-肝轴中的线粒体氧化和胆汁酸代谢,改善了氧化应激诱导的肠道细胞凋亡,导致肠道微生物群组成的重塑,这些代谢改善伴随着从肠道转运的肝脏中L-天冬氨酸水平的增加而发生。L-天冬氨酸的体外给药或在小鼠中灌胃显示出上述类似的有益代谢作用并有效改善MAFLD。总之,这些数据表明A. muciniphila的抗MAFLD活性与脂质氧化相关,并通过调节L-天冬氨酸的代谢改善肠-肝相互作用。A. muciniphila可能是MAFLD临床干预的潜在药物。
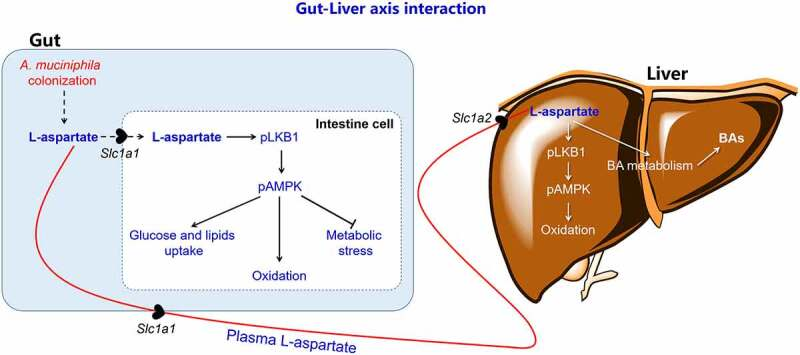
图 A. muciniphila改善HFC饮食诱导的肥胖小鼠MAFLD 的建议机制
研究报告原文详见:

文章仅供学术探讨,如需转载请注明出处。
 yzh@akkpro.com
yzh@akkpro.com


