欢迎您访问爱非克(深圳)生物科技有限公司
关键词:AKK菌、AKK菌格林汁
心房颤动(AF)是世界范围内最常见的心律失常之一,在普通人群中的患病率为1-2%。冷暴露是AF最重要的独立危险因素之一。据报道,环境温度每降低1℃,房颤的发病率增加3%。更重要的是,低温与AF患者的不良预后密切相关,包括心血管事件和全因死亡率的显著增加。然而,与寒冷相关的AF的潜在机制仍然很大程度上未知。
肠道微生物群由数千种细菌和数万亿微生物细胞组成,它们可能有助于人类宿主的心血管健康,并且当肠道微生物异常时,有助于包括AF在内的各种心血管疾病的发病机制。临床数据显示,房颤患者的肠道微生物功能失衡,代谢模式发生相关变化,这增加了差异肠道微生物组特征可用于识别房颤患者的可能性。肠道衍生的代谢物,如血浆氧化三甲胺(TMAO),与AF有关。已证明局部注射TMAO会增加正常犬的心房电生理学的不稳定性,并通过加剧自主神经重构来加剧快速心房起搏诱导AF模型中的急性电重构。更重要的是,TMAO作为AF患者血栓形成风险和缺血性卒中的独立预测因素已引起广泛关注。

- 研究结果
在该研究中,冷暴露导致大鼠对心房颤动(AF)的易感性升高,并降低了AKK菌丰度,口服AKK菌改善了冷暴露引起的促房颤特性。横断面临床研究证实寒冷大鼠模型中AKK菌丰度降低在人类受试者中重现,并被证明是与寒冷相关的AF的独立危险因素。
- 肠道菌群失调是与寒冷相关的AF的原因,口服AKK菌可防止大鼠患上与寒冷相关的AF,该研究为寒冷相关AF的机制提供了新的见解,这可能有助于寒冷相关AF的治疗和预防。
- 研究内容
- 人类队列研究
在A. muciniphila测试中,在哈尔滨医科大学第一附属医院医疗中心在冬季或夏季从初始AF或窦性心律(SR)患者收集粪便样本。11月至1月因AF或SR入院的患者称为冬季AF或冬季SR,而6月至8月因AF或SR入院的患者称为夏季AF或夏季SR。该研究中包括的AF患者被诊断为初始AF。冬季提供粪便样本的个人被要求连续暴露在室外寒冷环境中,每天至少2小时,持续两周以上。A. muciniphila测试的862名参与者中有521人被招募到研究中。其中,209人测量了A. muciniphila的粪便丰度被包括在最终分析中。
- 在TMAO测试中,采集了哈尔滨医科大学第一附属医院心血管病房住院患者的血液样本。从2019年1月到2019年12月,连续招募了1873名个体,并纳入了1305名测量血浆TMAO的受试者进行最终分析。排除标准预定义如下:检查时怀孕;过去三个月使用过的抗生素或益生菌;有心力衰竭、癌症或炎症性肠病史;过去一周有胃肠道疾病、呕吐、腹泻或非典型便秘;过去一周的饮食结构发生了显著变化。
- 动物实验
雄性SD大鼠(200-250g)适应性喂养一周后,采用完全随机化设计将大鼠随机分为两组:室温(RT)组升高至25±1℃,冷暴露(Cold)组在SPF条件下的温度控制和通风室中使用单独通风的笼子暴露于中度寒冷(4±1°C)中两周,n=7。Cold组大鼠通过饮用水给予1.0% 3,3-二甲基-1-丁醇(DMB,胆碱的结构类似物,抑制TMA的产生)2周。在抗焦亡实验中,通过腹膜内注射(2 g/kg/天)将 Necrosulfonamide(NSA,gasdermin D的直接化学抑制剂)给予Cold组大鼠2周,对照组大鼠给予相同量的缓冲液。在A. muciniphila补充实验中,Cold组大鼠每天分别以1×109 CFU/200 µL的剂量口服给予A. muciniphila或巴氏杀菌的A. muciniphila与厌氧PBS持续2周,对照组Cold鼠给予含2.5%甘油的PBS。
C57BL/6遗传背景中的Caspase1 floxed小鼠(Caspflox/flox)和Mef2c-Cre转基因小鼠,通过将Caspflox/flox小鼠与Mef2c-Cre转基因小鼠杂交,生成Mef2c-Cre驱动的心房和caspase1的右心室特异性缺失,产生Caspmef2c/mef2c和Caspflox/flox(对照)后代,然后进行冷暴露实验。
从不同的笼子收集冷暴露后房颤易感性显著增加的3只大鼠的粪便进行粪便微生物群移植(FMT)分析。
实验结束时,所有动物用戊巴比妥钠麻醉,进行电生理学分析测定AF的诱导率和持续时间。颈椎脱位处死后,收集心房组织进行免疫荧光染色分析和组织病理学分析。收集血浆样本和粪便样本进行LC-MS/MS分析。从粪便样本中提取微生物DNA进行16S RNA测序和微生物分析。
- 体外实验
从新生Sprague-Daw大鼠(1-3天大)的心脏中分离培养获得原代大鼠心肌细胞和成纤维细胞,然后分别用TMAO(10 μmol/L)或二甲基亚砜在37℃、5% CO2下培养48小时。
从SD大鼠的股骨中收集骨髓分离培养分化出巨噬细胞(BMDM)后,在存在或不存在TMAO(10 μmol/L)的情况下孵育48小时。
细胞共培养模型:将BMDM接种在6孔板中并用巨噬细胞集落刺激因子(M-CSF)处理6天以诱导M0巨噬细胞。然后,用TMAO处理M0巨噬细胞,同时将预处理的成纤维细胞/心肌细胞接种到具有2mL培养基的上室中。共培养48小时后,用含有1%蛋白酶抑制剂的RIPA试剂裂解心脏成纤维细胞/心肌细胞,提取总蛋白用于蛋白质印迹分析。MTT法测定细胞活力。收集巨噬细胞进行流式细胞仪分析。
- 研究内容
冷暴露通过诱导肠道菌群失调促进房颤
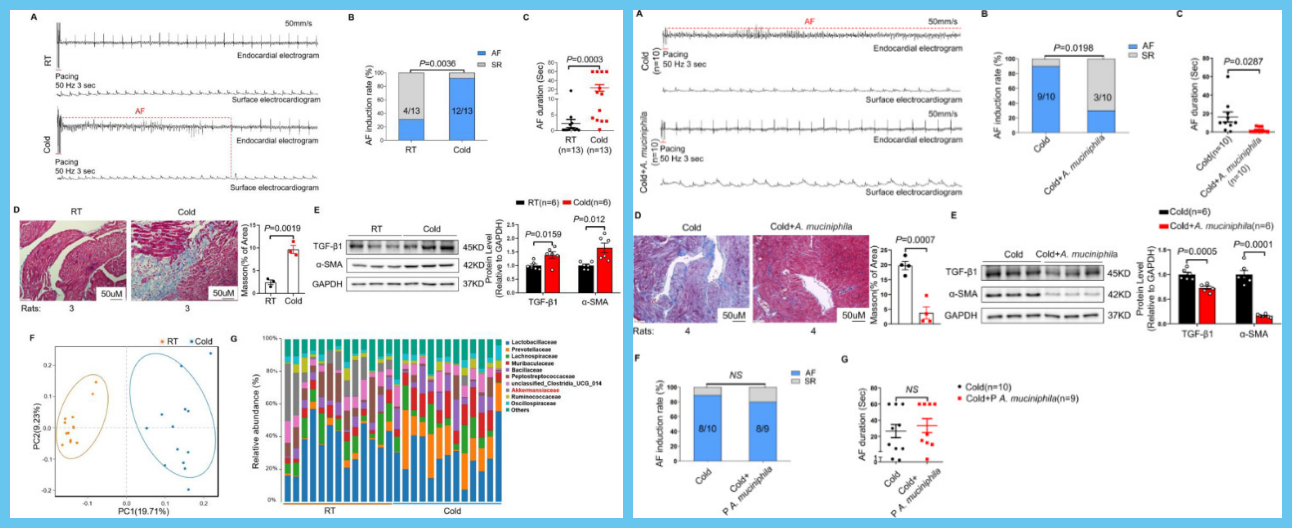
为分析冷暴露对大鼠房颤易感性的影响,该研究建立了冷动物模型,大鼠在冷温度(4 ± 1℃)下暴露2周,对照组大鼠在室温(25±1°C)下饲养。在RT组大鼠中短阵快速起搏很少引起AF,而在Cold组大鼠中通常引起AF。与RT组大鼠相比,在Cold组大鼠中AF诱导率和AF持续时间明显升高,这与临床研究一致。此外,在Cold组大鼠中观察到比在RT组大鼠中较大的心房胶原沉积和胶原体积分数。相应地,冷暴露上调了大鼠心房纤维化相关蛋白 TGF-β1和α-SMA的表达。越来越多的研究强调肠道微生物群在各种心血管疾病中的关键作用。同时,据报道肠道微生物群受到环境温度的影响。因此,该研究在寒冷暴露的第14天收集粪便样本进行16S rRNA分析。基于未加权UniFrac距离的主坐标分析(PCoA)揭示RT和Cold组大鼠的微生物群之间存在明显的聚类。测量α-多样性发现,群落丰富度显示两组之间没有统计学差异,而Cold组大鼠的群落多样性高于RT组大鼠。值得注意的是,在RT组和Cold组之间科水平的前10个差异微生物群的比例发生了显著变化,特别是Cold组中A. muciniphila的丰度显著低于RT组。
此外,还发现Cold组大鼠肠道通透性受损,这可以通过结肠组织中zonulin-1、occludin和claudin的表达降低来证明。
- 为研究微生物群变化在寒冷相关AF中的重要性,该研究将来自Cold或RT组大鼠的微生物群移植到野生型正常大鼠4周,并通过PCoA分析显示FMT效率。引人注目的是,移植Cold组菌群的大鼠显示AF的诱导率和持续时间显著增加,而移植RT菌群并未导致AF易感性的可检测变化。这些发现证实,与寒冷相关的AF是由异常的肠道微生物群介导的。
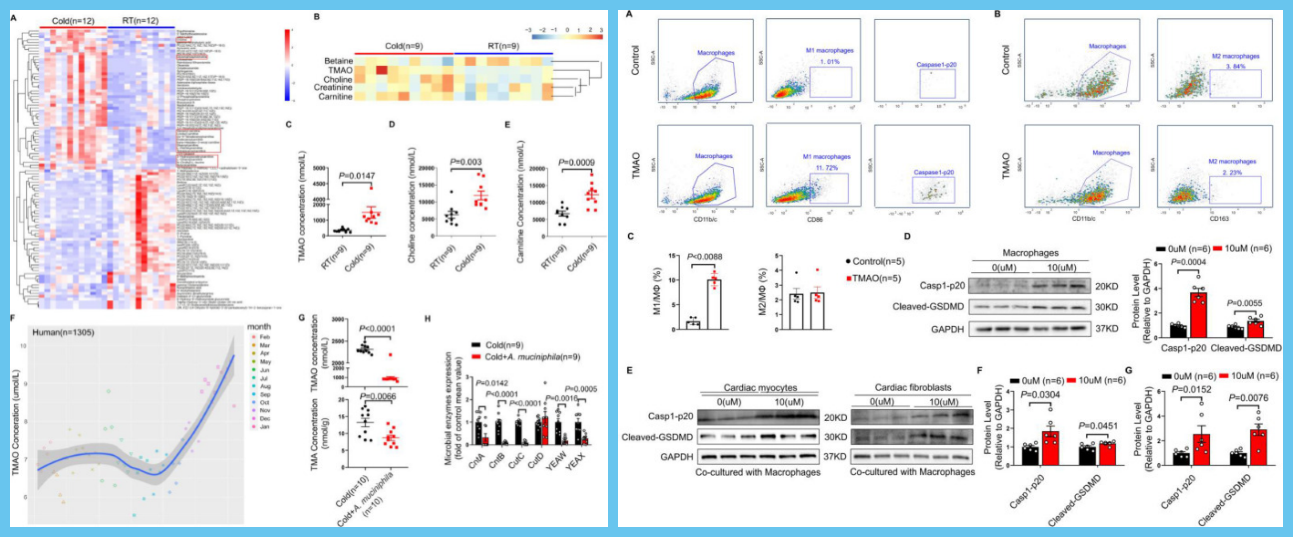
图左A. muciniphila通过抑制TMA合成来逆转冷暴露引起的TMAO升高&图右TMAO通过增强M1巨噬细胞浸润诱导心肌细胞和成纤维细胞的焦亡
为进一步证实细胞焦亡是寒冷相关性AF的关键机制,该研究将gasdermin D的直接化学抑制剂necrosulfonamide(NSA)通过腹腔注射(2g/kg/天)到Cold组大鼠。NSA处理抑制Cold 组大鼠Casp1-p20和cleaved-GSDMD的表达。令人惊讶的是,寒冷大鼠表现出增强的心房胶原蛋白沉积,而在接受NSA处理的寒冷大鼠中观察到纤维化减弱。此外,NSA处理降低了寒冷大鼠的AF易感性,这可以通过AF诱导性和AF持续时间的减少来证明。
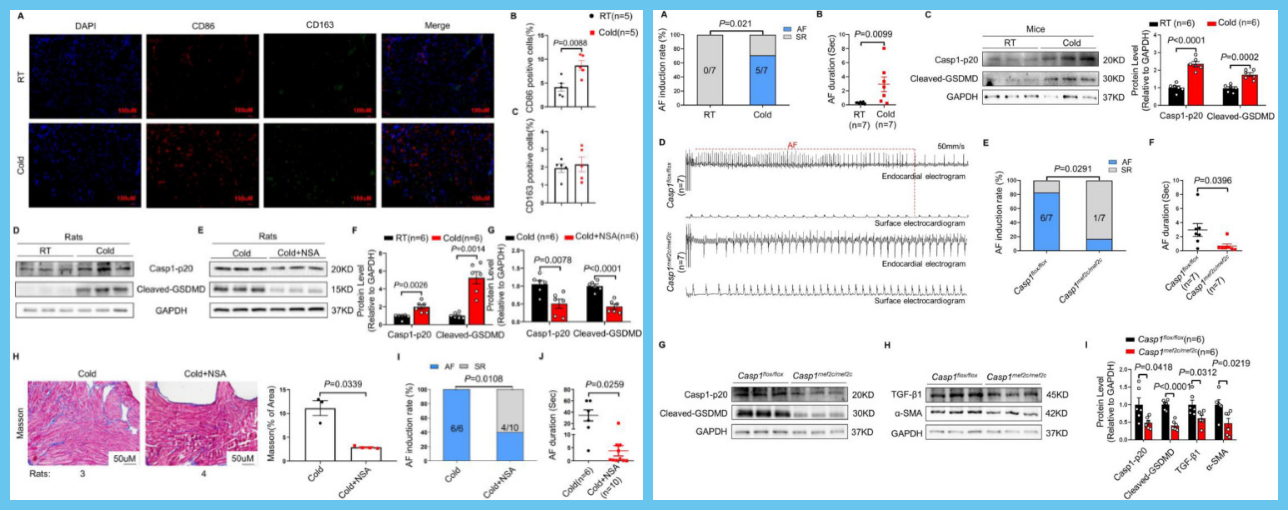
图 左NSA处理通过减轻心房焦亡来保护大鼠免受寒冷相关的AF&图右 Caspase1敲除通过抑制心房焦亡来保护小鼠免受与寒冷相关的AF
为了进一步证实细胞焦亡在寒冷相关AF中的关键作用,该研究使用了Casp1mef2c/mef2c小鼠模型,其中caspase1在心房和右心室有条件地缺失,蛋白质印迹证实心房中caspase1的成功敲除。结果发现,三周的冷暴露增加了野生型小鼠的AF易感性并加剧了心脏焦亡。然后,将Casp1flox/flox小鼠和Casp1 mef2c/mef2c小鼠暴露在寒冷中三周。结果表明,caspase1敲除降低了小鼠的AF诱导率和AF持续时间。同时,与Casp1flox/flox小鼠相比,Casp1mef2c/mef2c小鼠心房Casp1-p20和cleaved-GSDMD的表达显著降低。更重要的是,在Casp1mef2c/mef2c小鼠中观察到心房纤维化减轻。此外,DMB处理降低了感冒大鼠中Casp1-p20和cleaved-GSDMD的表达。总之,这些发现证实细胞焦亡在寒冷相关AF中的关键作用。
为进一步测试肠道菌群失调是否与寒冷相关的AF相关,该研究从冬季(冬季AF)或夏季(夏季AF)的AF受试者和冬季的窦性心律受试者(冬季SR)收集粪便样本或夏季(夏季SR)。值得注意的是,非度量多维标度(NMDS)揭示了冬季AF组与其他组之间的微生物组成存在显著差异。冬季AF组的肠道菌群丰富度(Chao1指数)明显高于其他组,而多样性(Shannon和Simpson 指数)则没有差异。测序数据显示,冬季AF组中A. muciniphila的丰度降低。随后,收集了103名冬季受试者和106名夏季受试者的粪便样本以证实A. muciniphila丰度的变化,qRT-PCR数据证实冬季受试者的A. muciniphila丰度低于夏季受试者。然而,SR组中A. muciniphila的丰度与AF组相当。为了进一步确定A. muciniphila在寒冷相关AF中的预测值,根据A. muciniphila丰度按A. muciniphila的三分位数分层检查了临床个体中AF的患病率。有趣的是,AF的患病率在冬季呈现出随A. muciniphila丰度而降低的趋势,但在夏季则没有,表明A. muciniphila丰度的降低与寒冷相关的AF有关。
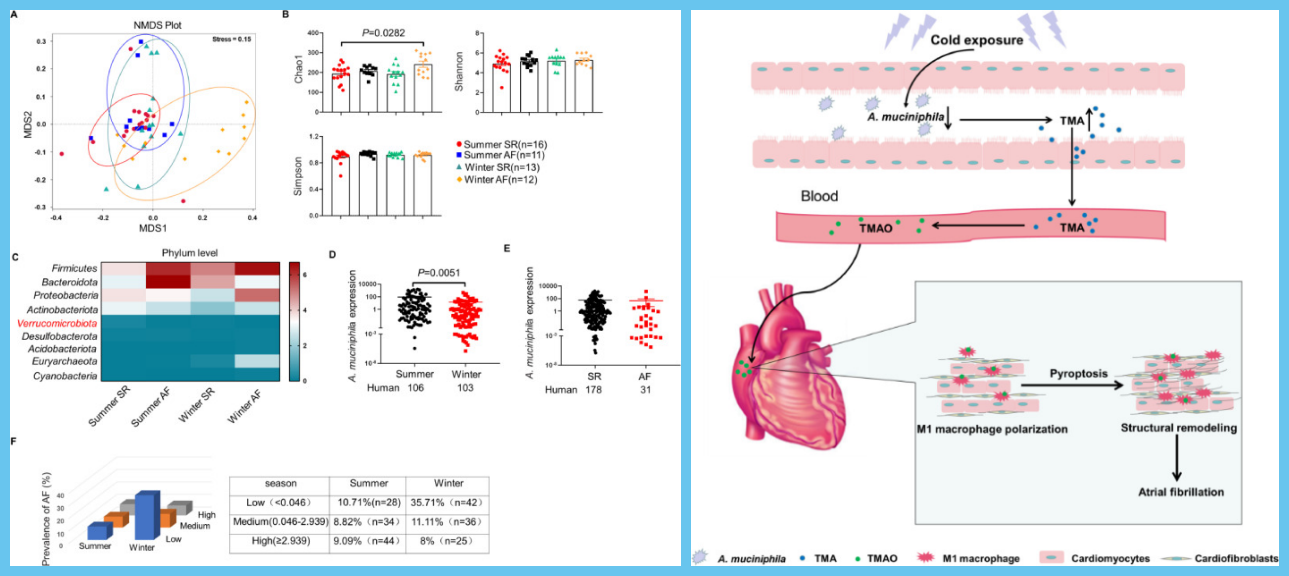
研究结论

文章仅供学术探讨,如需转载请注明出处。
 yzh@akkpro.com
yzh@akkpro.com


